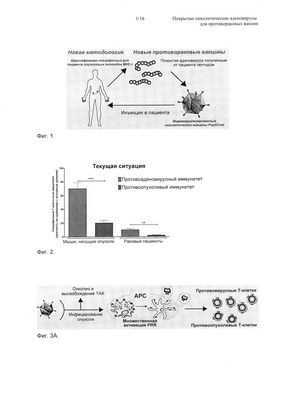
Исследователи из Нотр-Дама и их сотрудники объясняют, как выявление различий между мутантными (желтыми) и нормальными (оранжевыми) иммунными мишенями может помочь найти неоэпитопы, которые вызывают противораковые иммунные ответы
Команда ученых из Университета Нотр-Дам в сотрудничестве с исследователями из Университета Коннектикута объявила о результатах нового исследования по выявлению потенциальных целей для персонализированных противораковых вакцин. Бумага, "Геномное и биоинформатическое профилирование мутационных неоэпитопов раскрывает новые правила прогнозирования противоопухолевой иммуногенности," был недавно опубликован в Журнале экспериментальной медицины. Исследовательскую группу в Нотр-Даме возглавлял Брайан Бейкер, заместитель декана по исследованиям и аспирантуре, профессор химии и биохимии, и в нее входили Стивен Корчелли, доцент химии и биохимии, и аспирант Кори Эйерс.
"За последние 10 лет вакцинам против рака уделялось много внимания. Потенциал огромен, но реальный прогресс был медленным," сказал Бейкер.
Вакцины вводятся в организм для создания или усиления иммунного ответа на белковые антигены, которые отличаются от тех, которые обычно вырабатываются хозяином, например, из вирусных белков. Опухоли развиваются из-за мутаций в ДНК человека, вызывающих выработку мутировавших белков и неоантигенов, которые также отличаются от тех, которые вырабатываются хозяином. "Многие из этих неоантигенов приводят к разрушению иммунной системой раковых клеток на ранних стадиях," сказал Бейкер. "Однако в случаях установленного рака иммунный ответ недостаточен, но его можно повысить с помощью вакцин." Исследователям было сложно разработать вакцины против рака на основе неоантигенов, потому что они редки и могут варьироваться от человека к человеку. Кроме того, идентификация тех неоантигенов, которые достаточно отличаются от хозяина, чтобы вызвать реальный иммунный ответ, представляет собой еще одну проблему.
В исследовании обсуждаются два метода идентификации с относительно высокой точностью потенциальных неоантигенов для использования в качестве персонализированных противораковых вакцин. Комбинируя высокопроизводительное секвенирование генома и биоинформатику, команда Университета Коннектикута определила неоантигены, присутствующие в мышиных моделях рака. Затем группа Нотр-Дам объединила данные секвенирования с трехмерным структурным моделированием, чтобы предсказать, какие неоэпитопы больше всего отличаются от тех, что присутствуют в геноме нормальной мыши, что помогло идентифицировать неоэпитопы, которые были наиболее иммуногенными.
"Следующим шагом будет повторение этой методики с опухолями от больных раком человека," объяснил Бейкер. "Наша цель – однажды увидеть, как персонализированные вакцины играют ведущую роль в лечении рака. Благодаря достижениям в области секвенирования ДНК и компьютерного моделирования этот процесс можно было выполнить быстро – с момента секвенирования и анализа генома опухоли до производства коктейля вакцин – это можно было сделать за несколько недель."
"Это исследование очень захватывающее, потому что оно сочетает в себе иммунологию рака с персонализированной медициной, которые в настоящее время являются двумя из самых захватывающих областей биомедицинских исследований," Бейкер сказал. Исследовательские группы подали заявку на клиническое испытание с участием пациентов с раком яичников и планируют начать испытание этой зимой. Еще больше подчеркивая влияние науки Нотр-Дама, испытание будет возглавлять выпускник Нотр-Дама д-р. Энджи Куек из Университета Коннектикута, Центр комплексной онкологии им. Кэрол и Рэя Нэга. Он будет одним из первых в мире, кто протестирует индивидуализированную иммунотерапию рака на основе геномики, и первым в своем роде при раке яичников.