Основная причина потери функциональности пересаженных островков поджелудочной железы – их низкая способность создавать новые сосуды для транспортировки питательных веществ. Исследователи из Университета Барселоны и IDIBAPS провели исследование, в котором белок определен как потенциальный модулятор реваскуляризации островков поджелудочной железы.
В исследовании, проведенном на диабетических мышах с трансплантатом островков от других животных или островков человека, исследователи показали, что трансплантаты без этого белка имеют более высокую реваскуляризацию, что способствует жизнеспособности клеток. Также были восстановлены нормальный уровень сахара и толерантность к глюкозе.
Исследование координировали Рамон Гомис, профессор факультета медицины и медицинских наук Университета Барселоны, и Роза Гаса, исследователь в той же группе. Первым автором исследования, опубликованного в журнале Science Translational Medicine, является Уго Фигейредо, исследователь группы IDIBAPS.
Регенеративная медицина для лечения диабета 1 типа
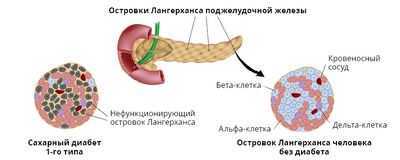
Одной из используемых стратегий лечения диабета 1 типа на основе регенеративной медицины является трансплантация островков поджелудочной железы. Островки образованы разными типами клеток и производят гормоны, такие как инсулин и глюкагон. При диабете 1 типа бета-клетки в островках, ответственных за выработку инсулина, выборочно разрушаются аутоиммунным процессом.
По этой причине трансплантация островков может восстановить физиологические функции у пациентов с этим типом диабета. "Хотя эта трансплантация проводится в некоторых центрах, она имеет ограничения, такие как постоянное введение иммунодепрессантов, и применяется в тех случаях, когда заболевание не контролируется должным образом. В настоящее время он показан в контексте трансплантации почки, и мы выбираем двойную трансплантацию сосудистой почки и поджелудочной железы," говорит Рамон Гомис, координатор исследования.
При этом возникают две основные проблемы: постоянное введение иммунодепрессантов и тот факт, что трансплантат не реваскуляризируется должным образом, что затрудняет транспортировку питательных веществ и кислорода. Этот недостаток делает островки нежизнеспособными и приводит к их гибели.
Регулярная среда для островков образована мощной сетью капилляров, отвечающих за поступление кислорода, гормонов и питательных веществ, а также за транспортировку выработанных гормонов в кровеносные сосуды. Во время процесса трансплантации островки отделяются от их сосудистой сети, и их правильная функция и выживание зависят от способности создавать новые сосуды для сосудистой системы в рецепторе.
"Имплантация островков реваскуляризована, но недостаточно быстро. В статье мы сосредоточились на получении достаточного количества сосудов для поддержания островков в оптимальном состоянии и повышении эффективности этой стратегии для лечения диабета 1 типа," отмечает исследователь Роза Гаса, координатор исследования.
Улучшение реваскуляризации
В ходе исследования ученые определили молекулярную мишень – фосфатазу PTP1B, которая сделает трансплантированные островки поджелудочной железы жизнеспособными. Результаты показывают, что ингибирование этого фермента, который присутствует во всех клетках, включая бета-клетки поджелудочной железы, способствует активности проангиогенного фактора роста VEGF, что позволяет создавать новые кровеносные сосуды. Следовательно, он обеспечивает более высокую реваскуляризацию лечения, что улучшает выживаемость и функциональность островков.
"Регуляция реваскуляризации вызывается гипоксией и недостатком питательных веществ, а ингибирование фосфатазы усиливает этот ответ. Когда раздражители исчезают, создание новых кровеносных сосудов прекращается," ноты Роза Гаса.
"Эта статья является подтверждением концепции, устраняющей одну из причин неудачной трансплантации островков поджелудочной железы. Существуют менее специфические ингибиторы PTP1B и фосфатаз, и поэтому следующим шагом будет тестирование этих ингибиторов в трансплантате островков на людях и оценка его успешности," заключает Рамон Гомис.